Postagem realizada com base no capítulo 2 do excelente livro de química orgânica dos autores Jonathan Clayden, Nick Greeves e Stuart Warren.
A química orgânica estuda como os átomos (carbono, hidrogênio, oxigênio, nitrogênio e outros) estão ligados formando estruturas moleculares estáveis e como estas estruturas mudam no decorrer das reações químicas.
Para desenhar estruturas atômicas é necessário se realista, econômico e claro. Ou seja, desenhar a estrutura molecular o mais próximo da realidade (lembrando que moléculas ocupam um espaço tridimensional e sempre que possível os ângulos entre os átomos devem ser mostrados), desenhar as ligações carbônicas como retas em que os ângulos e as pontas indicam um carbono (por exemplo, alcanos devem ser desenhados em zigue-zague) com os hidrogênios ocultos na cadeia de hidrocarbonetos, pois eles podem ser deduzidas já que todo carbono faz quatro ligações, possibilitando escrever a molécula mais rapidamente.
As estruturas tetraédricas são tridimensionais (3D), entretanto devem ser escritos num papel que e bidimensional (2D). Assim, o CH4 é um carbono tetraédrico (uma pirâmide de base triangular) e deve ser desenhado mostrando esta estrutura 3D. Assim, para ilustrar isso nas figuras abaixo, a ligação químicas representadas com uma reta indica os hidrogênios que estão no plano do papel e os hidrogênios que estão atrás do papel estão com uma ligação pontilhada e os hidrogênios que estão para frente do papel tem uma ligação com uma linha que vai engrossando conforme se aproxima do hidrogênio. O ângulo tetraédrico é de 109,5º.

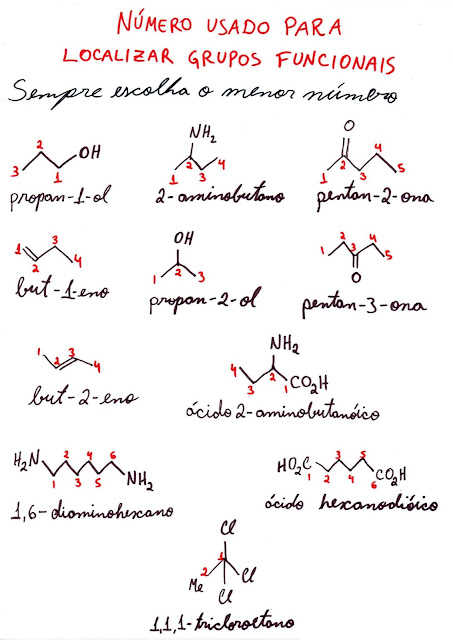
Para facilitar a comunicação em textos sobre moléculas químicas torna-se necessário nomear estas estruturas. Começando pelo esqueleto carbônico:
Nomenclatura de cadeias carbônicas
|
||||
Número de carbonos
|
Nomenclatura para a molécula
|
Fórmula
|
Abreviação
|
Nome do alcano (=cadeia+H)
|
1
|
met
|
-CH3
|
Me
|
metano
|
2
|
et
|
-CH2CH3
|
Et
|
etano
|
3
|
prop
|
-CH2CH2CH3
|
Pr
|
propano
|
4
|
but
|
-(CH2)3CH3
|
Bu
|
butano
|
5
|
pent
|
-(CH2)4CH3
|
pentano
|
|
6
|
hex
|
-(CH2)5CH3
|
hexano
|
|
7
|
hept
|
-(CH2)6CH3
|
heptano
|
|
8
|
oct
|
-(CH2)7CH3
|
octano
|
|
9
|
non
|
-(CH2)8CH3
|
hexano
|
|
10
|
dec
|
-(CH2)9CH3
|
decano
|
|
No caso do grupo metil, etil, propil e butil eles podem ser abreviados na molécula desenhada, aparecendo com duas letras como os elementos químicos (Me, Et, Pr, Bu), estes são chamados elementos carbônicos.
O anel aromático, anel benzênico pode ser abreviado como Ar, entretanto, já existe um elemento químico com esse símbolo, o argônio. Entretanto não existem compostos carbônicos com argônio, então sempre que você ver o símbolo Ar em um composto carbônico é a indicação de um anel aromático.
Um tipo específico de anel benzênico é o fenol, que tem um dos hidrogênios do anel substituído por uma hidroxila (OH). Quando apenas um hidrogênio do anel benzênico e substituído por outro átomo ou outra cadeia carbônica, chamamos essa estrutura de fenil, que é abreviado por Ph.
Isômeros tem um mesmo número de átomos, unidos de diferentes formas.
Carbonos primários (n-), secundários (sec-), terciários (tert-) e quaternários.
Os esqueletos carbônicos não influenciam muito na ação dos compostos orgânicos,
eles servem praticamente para suportar os grupos funcionais que é o que mais
influencia nas propriedades físicas e químicas das moléculas. Grupos
funcionais: alcano (apenas ligações simples
entre os carbonos), alqueno (pelo menos uma ligação dupla entre carbonos),
alquino (pelo menos uma ligação tripla entre carbonos), álcool (R–OH), éter (R1
– O – R2), amina (R–NH2),
nitro (R–NO2), aleto de alquila (R-halogênio: R–F, R–Cl, R–Br, R–I),
aldeído (R–CHO), ácido carboxílico (R-CO2H), éster (R1 – CO2 R2), amida
(R éter (R–CONH2 ou R1 –
CONHR2 ou R1 – CONR2
R3 ) , nitrila ou cianila (R–CN), acyl chloride (R–COCl), acetal (O –
C – O).
Níveis de Oxidação
Todos dos grupos funcionais são diferentes, entretanto podemos agrupá-los de acordo com propriedades e número carbonos ligados a átomos diferentes de carbono e hidrogênio (heteroátomos). Alguns grupos funcionais podem ser tranformados em outros sem a necessidade de agentes redutores ou oxidantes, estes grupos funcionais que podem ser intercambiáveis tem o mesmo número de oxidação, ou seja, o mesmo número de heteroátomos.
Por exemplo: ácidos carboxílicos, esteres e amidas podem ser transformados uns nos outros usando reagentes simples como água, álcool ou aminas na presença de catalizadores, entretanto para transformá-los em aldeído ou álcool é necessário um agente redutor (reagente que adiciona átomo de hidrogênio).
Nomenclatura
Nomenclatura:
metano, etano, propano, butano, pentano, hexano,
octano, nonano, decano
An: ligação simples entre carbonos, o: apenas carbono
e hidrogênio















Nenhum comentário:
Postar um comentário